客户文献分享| IF=14.612,基于酶催化的Asp-Phe-Tyr三肽聚合反应癌症免疫疗
信息来源:金开瑞 作者:genecreate 发布时间:2021-05-17 15:48:02
本期解读
题目:A Strategy Based on the Enzyme-Catalyzed Polymerization Reaction of Asp-Phe-Tyr Tripeptide for Cancer Immunotherapy期刊:JOURNAL OF THE AMERICAN CHEMICAL SOCIETY
影响因子:14.612/Q1
合作技术:iTRAQ定量蛋白组学
一、研究背景
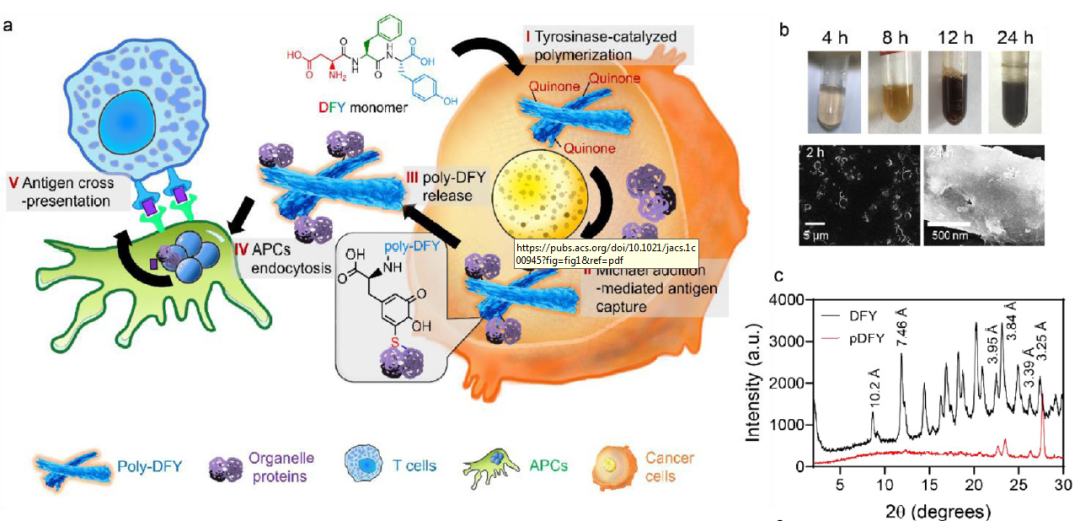
释放免疫系统的力量被认为是治疗癌症的重要策略。尽管大多数癌症都表达肿瘤特异性抗原,但免疫疗法仍是保守的,反应低且不良反应频繁。一个主要原因是癌症已经获得了抑制抗原呈递的能力。约70-95%的人类癌细胞下调与抗原呈递相关的蛋白质的表达。这些蛋白质的系统性缺乏促使癌细胞逃脱免疫识别。激活免疫系统的努力主要集中在使用拮抗剂或抑制剂靶向某些蛋白质上。但是,单靶标药物的功效是有限的,而免疫疗法为癌症提供了一个有前景的治疗策略。然而,即使在高抗原负担的肿瘤中,全身抑制抗原提呈仍然极大地限制了免疫治疗的应用。在此,研究者构建了一种基于功能三肽Asp-Phe-Tyr (DFY)的肿瘤蛋白工程系统,该系统可以自动收集和传递靶向细胞的免疫肿瘤蛋白到免疫细胞中。通过酪氨酸酶催化聚合,DFY三肽选择性地聚集在酪氨酸酶高表达的黑色素瘤细胞中。然后将富含醌的中间体与肿瘤特异性蛋白通过Michael加成共价连接,形成携带肿瘤蛋白的微纤维,该微纤维可被抗原提呈细胞吞噬,并表现出肿瘤抗原特性以增强免疫效果。在抗原递呈不足的黑色素瘤细胞中,该系统可以成功地富集和运输含有肿瘤抗原的蛋白质到免疫细胞。此外,在小鼠黑色素瘤的体内研究中,DFY三肽经皮传递抑制肿瘤生长和术后复发。
二、技术路线
聚合肽筛选鉴定——聚合肽DFY作用机制解析——DFY作用下功能蛋白差异性分析——肿瘤蛋白交联pDFY的免疫激活机制解析——肿瘤模型DFY抗癌作用验证
三、实验结果
1. 酪氨酸酶催化聚合DFY。
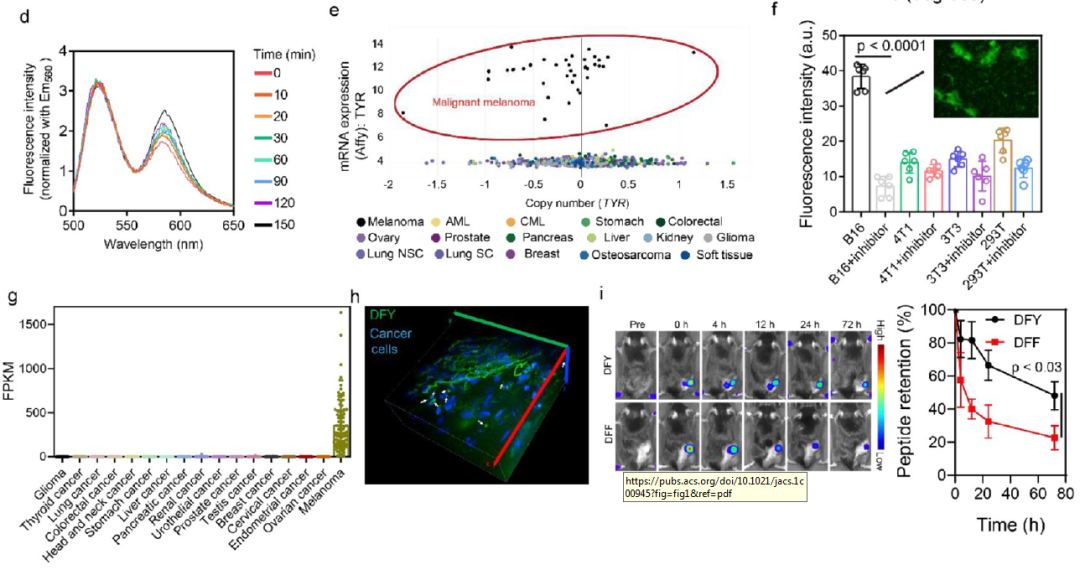
首先,研究者筛选得到一种可被酪氨酸酶催化聚合的肽DFY(Asp-Phe-Tyr),并观察到在聚合过程中产生了不溶性黑色沉淀物,利用倒置显微镜和扫描电子显微镜(SEM)观察均表明是由DFY聚合成的微纤维(图1b和图1b)。然后,研究者研究了各种细胞系中酪氨酸酶基因(TYR)表达的差异,基于CCLE数据库(https://portals.broadinstitute.org/ccle)分析了TYR基因在740个细胞系中的表达水平,结果表明,与其他癌细胞分型相比,黑色素瘤细胞系表现出最高的TYR基因表达量(图1e)。此外,研究了酪氨酸酶过表达的黑色素瘤细胞中DFY的胞内聚合反应(图1f),结果表明DFY在黑素瘤细胞中的聚合是酪氨酸酶依赖性的。此外,研究者验证了DFY的聚合是否可以在体内原位诱导。将DFY和不可聚合肽(Asp-Phe-Phe,DFF)注射到小鼠癌旁组织中以观察其在肿瘤中的清除情况。如图1i所示,注射的DFY比DFF在肿瘤位置停留的时间更长,相比之下,大多数DFF在肿瘤中被快速清除了,因此推测DFY能在肿瘤组织中特异性聚合。

2. DFY的胞内蛋白捕获。
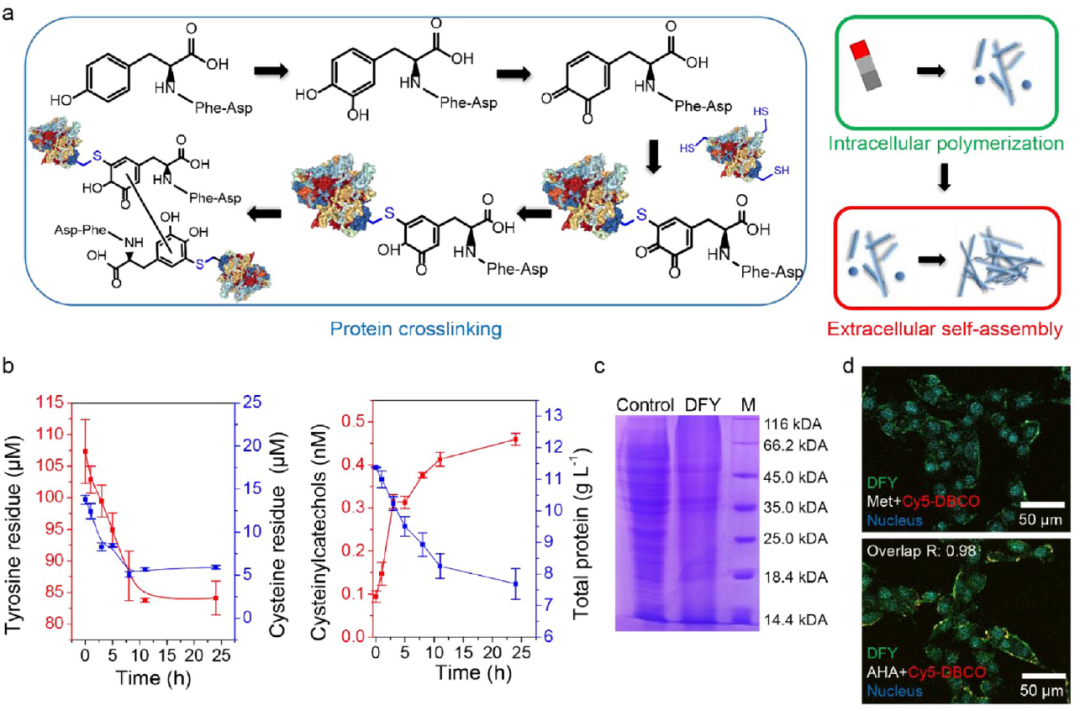
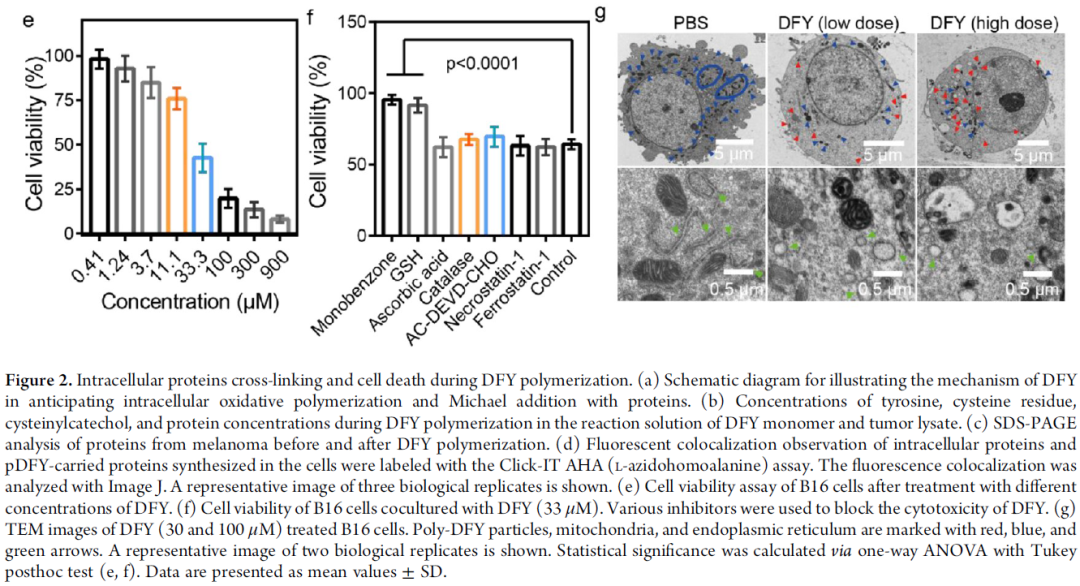
研究者通过MTT分析表明,DFY在33μM的浓度下可抑制小鼠B16细胞的增殖达57%(图2e),在与各种B16细胞抑制剂孵育后,发现单苯甲酮(酪氨酸酶抑制剂)和谷胱甘肽(GSH)均可将B16细胞从DFY聚合引起的细胞死亡过程中拯救出来(图2f)。Ac-DEVD-CHO(凋亡抑制剂),ferrostatin-1(促肥大症抑制剂),necrostatin-1(坏死性抑制剂),TBHQ和BHA(醌氧化还原酶诱导剂)却无法挽救DFY对细胞的伤害。得出的结论是,单苯甲酮和谷胱甘肽的解毒作用归因于GSH和DFY之间的迈克尔加成。通过荧光显微镜观察,发现长期培养后,微纤维从细胞中释放出来(图4Sd,e)。实验证明DFY收集靶细胞的胞内蛋白,并以类似于坏死的方式将它们转运出细胞,并伴随DFY聚合诱导的细胞死亡。因此,由pDFY携带的肿瘤蛋白的释放可能刺激随后的抗原触发的免疫反应。
3. 交联蛋白的蛋白质组学研究。
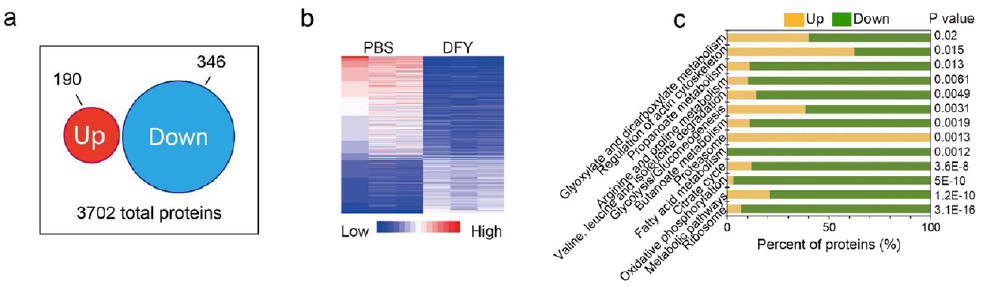
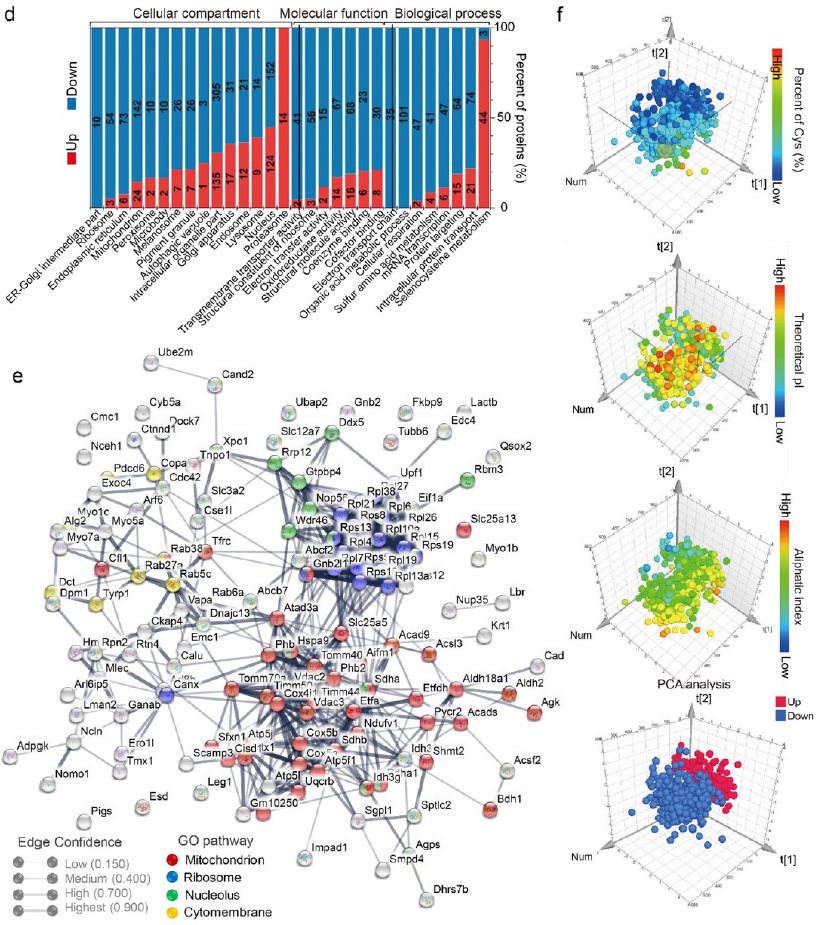
由于蛋白质的免疫原性因蛋白质而异,研究者研究了通过抗原工程系统收集的蛋白质类型,与金开瑞合作的串联质谱用于定量分析蛋白质含量。如图3a,b和S5所示,在DFY聚合后,确定了190个上调蛋白和346个下调蛋白(倍数变化1.5和P <0.05,超几何测试)。然后通过GO数据库富集分析了这些差异蛋白的功能。结果表明,这些蛋白质大多数与细胞代谢(氨基酸代谢,糖代谢),能量供应(糖酵解,有氧呼吸)和蛋白质合成(核糖体)相关(图3c)。发现这些蛋白质在功能上涵盖了细胞最重要的生物学功能(图3d)。差异蛋白主要来自核糖体,线粒体,细胞核和高尔基体。此外,通过STRING功能蛋白缔合网络研究了DFY聚合后减少的蛋白质之间的相互作用(图3e)。来自细胞器的蛋白质,特别是核糖体,线粒体和细胞核中的蛋白质,形成紧密的簇。该结果表明DFY可以特异性地交联来自这些细胞器的蛋白质,从而导致这些蛋白质的显着减少。另外,作为专业的产生黑色素的细胞器,还分析了在DFY处理的黑色素瘤细胞中黑色素体的蛋白质表达(图S5)。GO富集分析的结果表明,用DFY处理后,黑素体中的大多数相关蛋白也被下调。使用主成分分析(PCA)分析了Cys含量,理论等电点和差异蛋白质脂肪族指数三个指标(图3f),该结果表明被下调的蛋白质可以被DFY结构结合或化学交联。从实验上观察到,DFY处理可抑制线粒体功能,抑制蛋白质合成并损害细胞骨架形成(图S6)。这些实验结果与理论推测吻合良好。

4. 肿瘤蛋白交联pDFY的免疫激活。
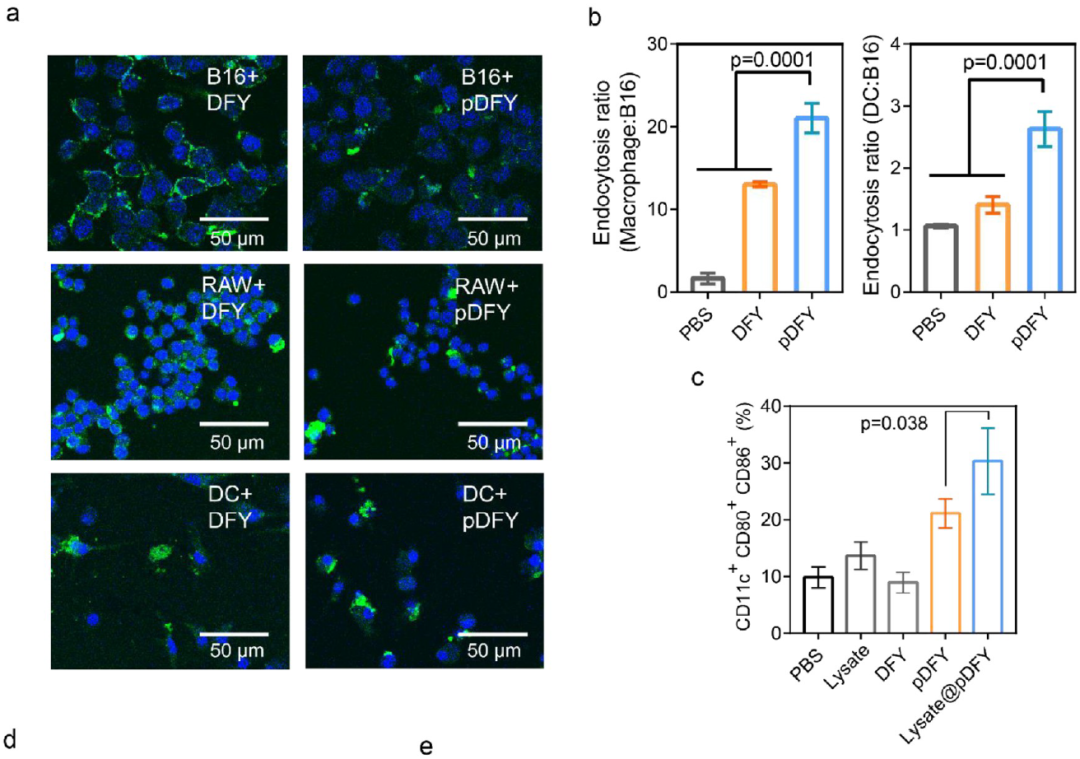
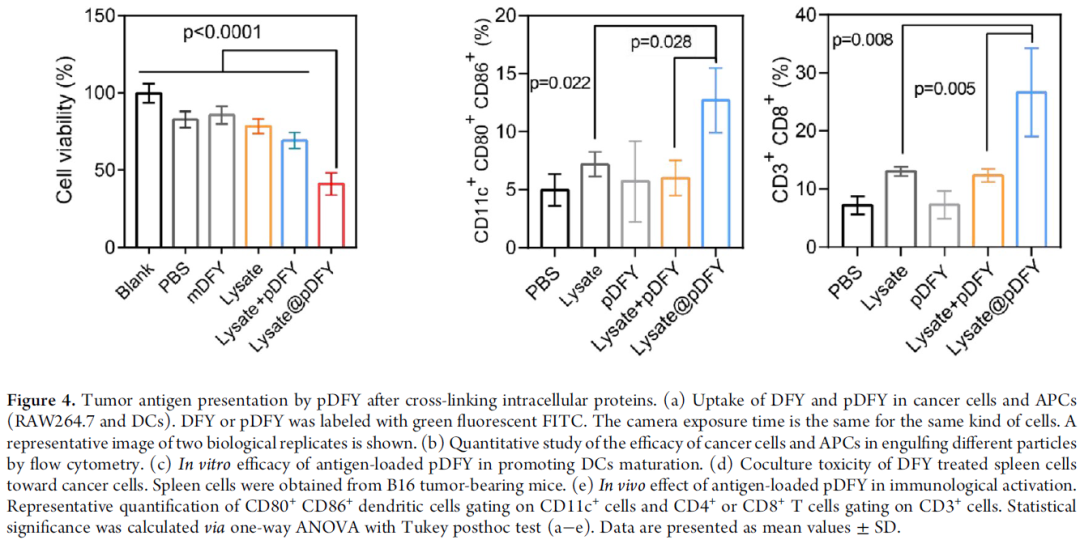
为了研究B16细胞释放的纤维是否可以被APC吞噬,通过共聚焦荧光显微镜和流式细胞术检查了B16和APC(RAW264.7和DC)对DFY或pDFY的摄取(图4a,b)。荧光成像表明DFY在各种细胞中积累,但pDFY倾向于被APC吞噬。该观察证明,纤维携带的抗原蛋白更倾向于递送至APC。为了阐明pDFY携带的肿瘤蛋白是否能增强免疫反应,用流式细胞仪进一步分析了裂解物蛋白交联的pDFY在DCs成熟中的能力(图4c)。与裂解物组相比,裂解物+ pDFY在DC的成熟度上增加了2.3倍。此外,与裂解物+ pDFY相比,裂解物@pDFY诱导的DC成熟也更为显着(P = 0.0002)。然后将B16蛋白交联的经pDFY处理的B16细胞和脾细胞以1:10的比例共孵育,以研究智能抗原工程系统引发针对癌细胞的特异性免疫反应的能力(图4d),研究发现经裂解物@pDFY处理的脾细胞消除了59.3%的B16细胞。相反,裂解物或裂解物+ pDFY处理的脾细胞的混合物仅杀死了不到30%的B16细胞。携带肿瘤抗原蛋白的裂解物@ pDFY成功触发了针对B16细胞的特异性免疫杀伤。在此基础上,考虑到pDFY的佐剂作用和交联蛋白的强免疫原性,抗原工程系统可作为黑色素瘤治疗的免疫增强疫苗型材料。最后,经B16荷瘤小鼠皮下药物注射研究,证明了由于某些功能蛋白被裂解物@ pDFY富集,裂解物@ pDFY可以成功激活体内抗癌免疫反应。
5. DFY在不可切除黑色素瘤中的抗癌作用。
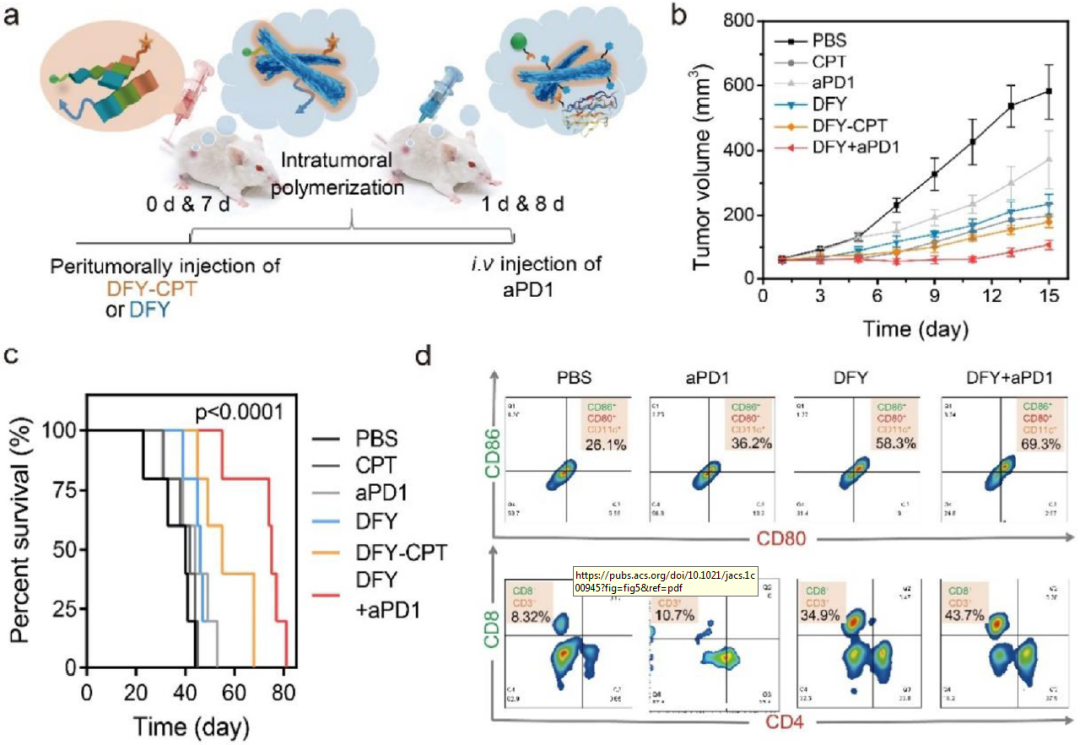
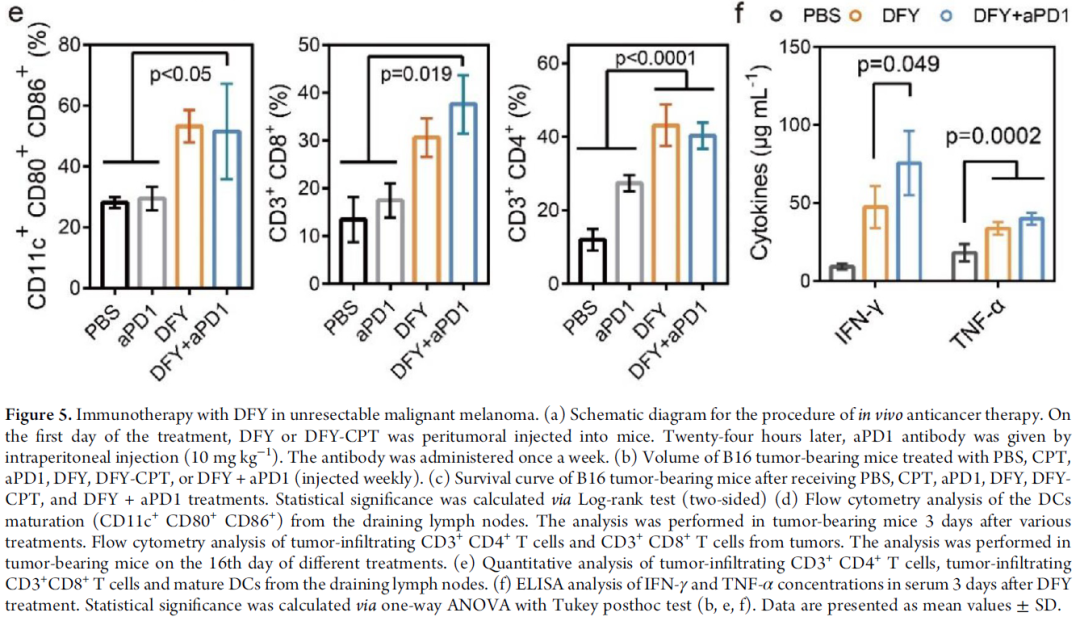
随后,研究者对抗原工程系统的肿瘤抑制能力进行了分析。抗PD1抗体(aPD1)或化学治疗药物已与基于DFY的抗原工程系统结合用于治疗B16荷瘤小鼠(图5a)实验结果表明DFY + aPD1的治疗抑制了91%的肿瘤生长。研究者还记录了各种治疗后小鼠的存活率(图5c)。在所有组中,用DFY + aPD1处理的小鼠的存活时间最长。该结果表明,肿瘤周围注射DFY不仅可以收集可能含有肿瘤抗原的肿瘤蛋白,而且可以将免疫原性肿瘤蛋白递送至APC并引起随后的CTL激活以抑制肿瘤进展。酶联免疫吸附试验(ELISA)显示,DFY + aPD1处理后,包括干扰素γ(IFN-γ)和肿瘤坏死因子α(TNF-α)在内的免疫激活标记物增加(图5f)。
6. DFY经皮给药治疗黑色素瘤。
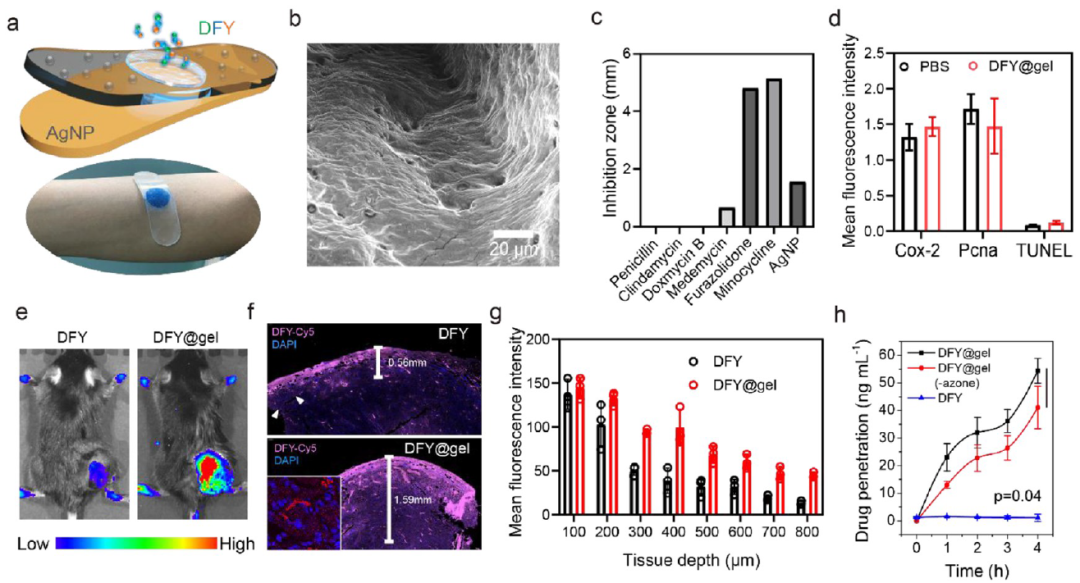
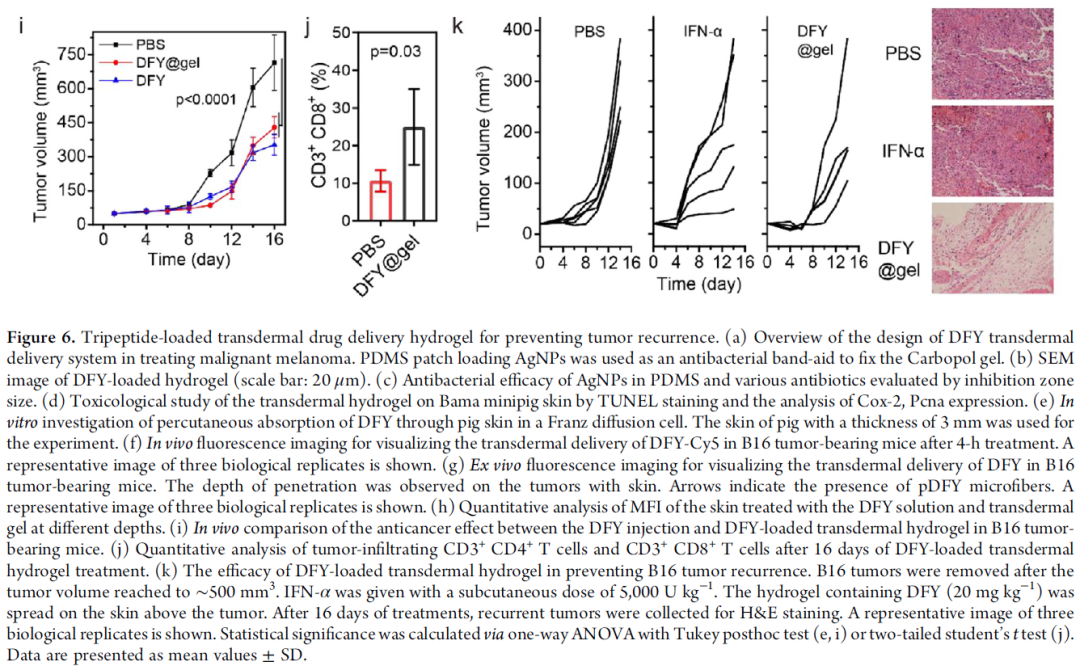
研究者将凝胶状的DFY @ gel作为一种透皮治疗系统,粘附在皮肤上时释放DFY。如图6g所示,在相同深度下,用DFY @ gel治疗的肿瘤的平均荧光强度(MFI)高于DFY。使用V-C扩散池和荧光光谱仪研究了分离的猪皮中DFY @ gel的透皮吸收。与游离DFY相比,DFY @ gel的透皮渗透提高了1.5倍(图6h)。然后通过测量肿瘤体积评估DFY @ gel抑制肿瘤生长的能力(图6i)。在为期16天的实验中,DFY @ gel显示出与DFY(腹膜内注射)相似的治疗效果。IFN-α在临床上用于术后黑色素瘤的治疗。与临床方案相比,评估了DFY @ gel的治疗效果。IFN-α和经皮凝胶治疗均显着抑制了肿瘤的复发。该结果表明透皮DFY @ gel在预防黑素瘤复发方面具有与临床上使用的IFN-α几乎相同的治疗效果。
四、小结
在这项研究中,研究者设计了一种基于肽的肿瘤蛋白工程系统,该系统对黑素瘤治疗表现出强大的免疫原性。一旦进入恶性黑色素瘤细胞,该三肽进行酪氨酸酶催化的氧化聚合。同时,通过迈克尔加成反应还捕获了来自细胞核,线粒体和核糖体的高免疫原性功能蛋白,这引起了类似于坏死的快速细胞死亡。随后,肿瘤蛋白交联的pDFY从垂死和破裂的癌细胞中释放出来,形成的聚集纤维更易于被APC内吞。因此,设计的肿瘤蛋白质工程系统成功地收集了免疫原性蛋白质并将其递送至APC,并表现出辅助作用以增强免疫应答以消除肿瘤。DFY的经皮免疫疗法在小鼠和小型猪模型中也显示出高效率和高生物相容性,并显着延长了肿瘤小鼠的存活时间。在可切除的黑色素瘤中,发现DFY@gel具有与临床IFN-α治疗相似的复发预防效果。
了解金开瑞iTRAQ定量蛋白质组学技术:https://www.genecreate.cn/iTRAQ/
最新动态
-
03.11
同为抗体,为什么一抗看“抗原种类”,二抗却看“一抗种属”?
-
03.11
J Nanobiotechnology(IF=12.6):蔓越莓“纳米邮差”递送麦角甾醇,重启早衰卵巢功能!
-
02.27
没有抗体?不是模式植物?DAP-seq照样搞定你的TF靶基因!
-
02.27
高分研究的共同选择:三篇权威文献背后的ChIP实验工具解析
-
02.27
表观遗传学进入“多维验证”时代,这些疾病机制再也藏不住了!
-
02.27
“药食同源”顶刊思路(IF=10.5)!来源鉴定+活性追踪+体内验证,全面解析无花果来源外泌体抑制乳腺癌骨转移的双重机制!
-
02.27
千年古方,纳米新生:科学家破解半夏如何“指挥”免疫细胞对抗肺癌!
-
01.29
技术跨界联用:表观遗传学进入“多维验证”时代,这些疾病机制再也藏不住了!文末有惊喜活动!
-
01.29
机制研究的金标准:金开瑞RIP/RNA pull-down试剂盒获多篇顶刊研究认可!
-
01.29
想测结合常数,但样本太珍贵?来试试MST技术










