Heliyon|武大中南医院王炜煜团队:揭示何首乌外泌体纳米颗粒抗肝癌分子机制
外泌体——这颗生命科学领域的“明星分子”,正以惊人的速度改写疾病治疗的未来!我司合作发表的一篇研究何首乌外泌体抗肝癌机制的文章,在《Heliyon: An Open Access Journal》期刊上亮相。从中药植物到跨界抗肿瘤,给我们提供了中药外泌体在癌症治疗的全新思路。
一、文献背景与创新突破
本文题为《Molecular anti-tumorigenic mechanism of Radix Polygoni Multiflori-derived exosome-like nanoparticles》本研究首次从传统中药何首乌(Radix Polygoni Multiflori, RPM)的汁液中分离出外泌体样纳米颗粒(ELNs),并证实其具有显著的抗肝癌活性。此前,植物ELNs的研究多集中于柠檬、山药、苦瓜等,而RPM作为具有悠久药用历史的中药,其ELNs的分离与功能探索填补了该领域的空白。
✨创新突破:全球首次从何首乌中分离出外泌体样纳米颗粒(ELNs),证实其通过调控细胞周期基因(如Cdkn1a、Cdc20)显著抑制肝癌细胞增殖与迁移,体内靶向富集于肝脏!
✨科学价值:开创何首乌“中药-外泌体”跨界抗肿瘤新模式,为天然药物开发提供全新载体。
二、主要研究思路
(1)首次从何首乌(RPM)中分离ELNs
通过差异离心和超速离心将ELN分离并从新鲜RPM汁液中提取ELNs。此方法避免了化学试剂的干扰,保留了ELNs的天然生物活性。通过对外泌体进行鉴定,发现RPM-ELNs平均粒径159.5 nm(NTA分析),符合外泌体典型的粒径大小范围,而且具有明显的杯状结构。除此之外泌体PKH26染色实验证明,RPM-ELNs可以被细胞有效吸收。
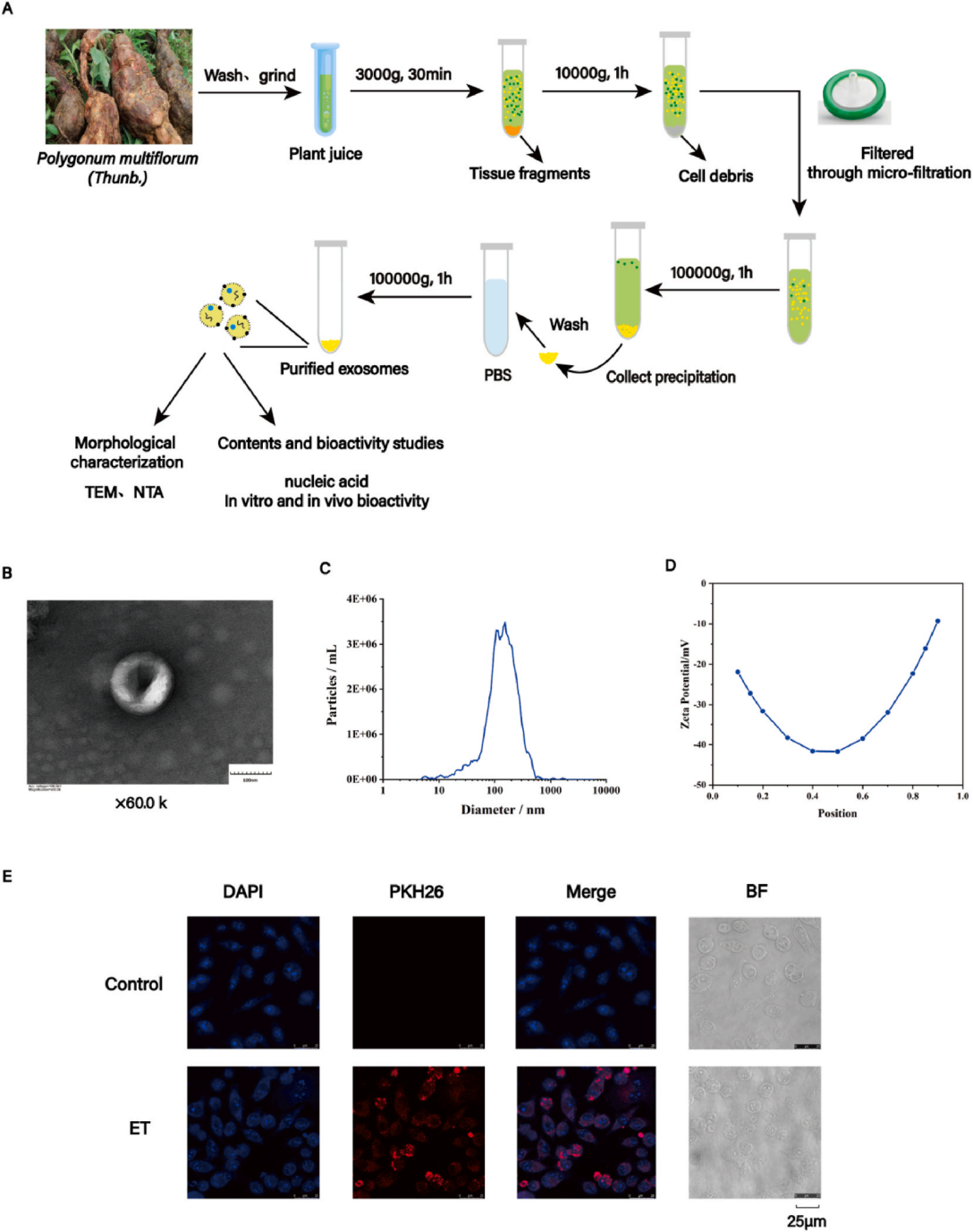
图1. 源自RPM的外泌体样纳米颗粒(ELN)的表征和细胞内在化
(2)多维度验证抗肿瘤机制
通过体外细胞实验(增殖、凋亡、迁移抑制)结合增殖抑制:CCK-8实验显示,RPM-ELNs(10⁹ particles/mL)处理24-72小时后,SMMC-7721肝癌细胞活力显著下降(图2A-B)。克隆形成实验显示ELNs显著减少细胞克隆形成数量(图2C-D),表明其长期抑制肿瘤细胞增殖的能力。流式细胞术显示,ELNs处理组早期凋亡(Annexin V+)和晚期凋亡(PI+)细胞比例显著升高(图2E-F)。
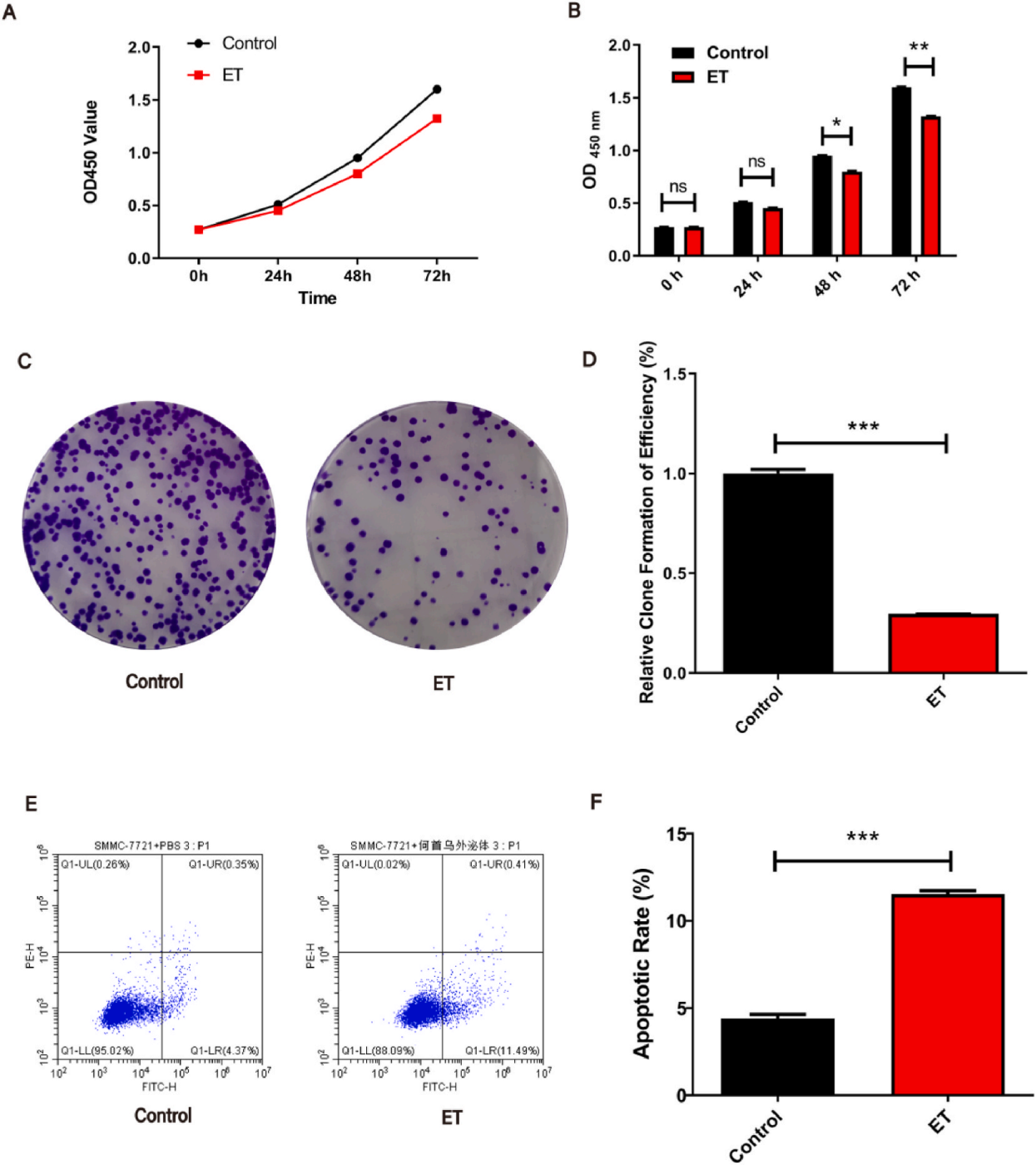
图2.RPM-ELNs调节SMMC-7721细胞的增殖和凋亡
(3)分子机制解析
RNA测序(RNA-seq)和生物信息学分析,系统揭示了RPM-ELNs通过调控细胞周期相关基因(如Cdkn1a、Cdc20)和信号通路(如HIF-1、FoxO)发挥抗肿瘤作用的分子机制。这种“表型-基因-通路”的多层次研究模式,为天然产物抗肿瘤机制解析提供了范式。
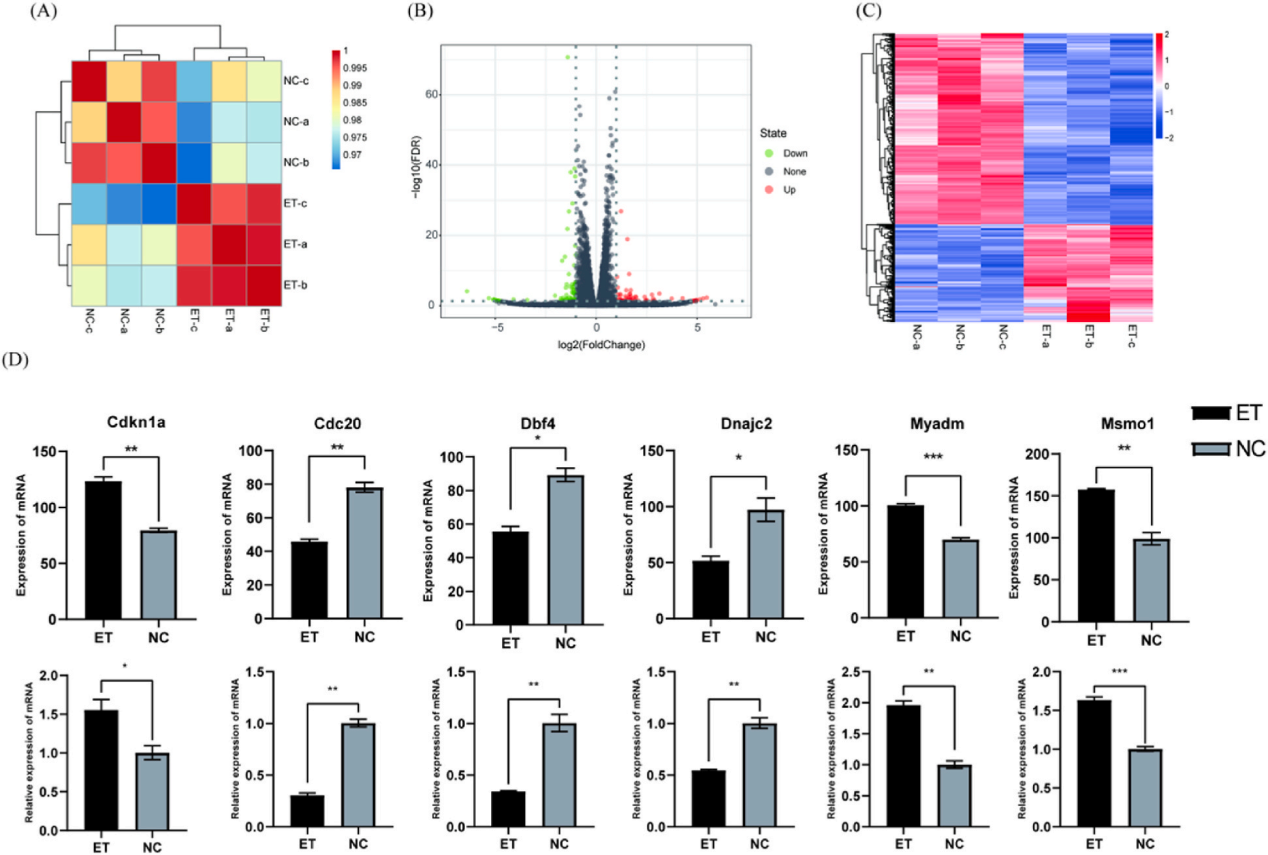
图3.RPM-ELNs的抗癌机制的分析
(4)体内靶向性验证
通过外泌体体内示踪实验,发现RPM-ELNs在小鼠体内主要富集于肝脏,其次是脾脏和肺脏,证明了何首乌外泌体具有天然肝靶向性。这一特性可能归因于肝脏网状内皮系统对纳米颗粒的主动摄取,或ELNs表面特定蛋白(如整合素)与肝细胞受体的相互作用,该发现为后续开发肝癌特异性纳米药物提供了重要依据。
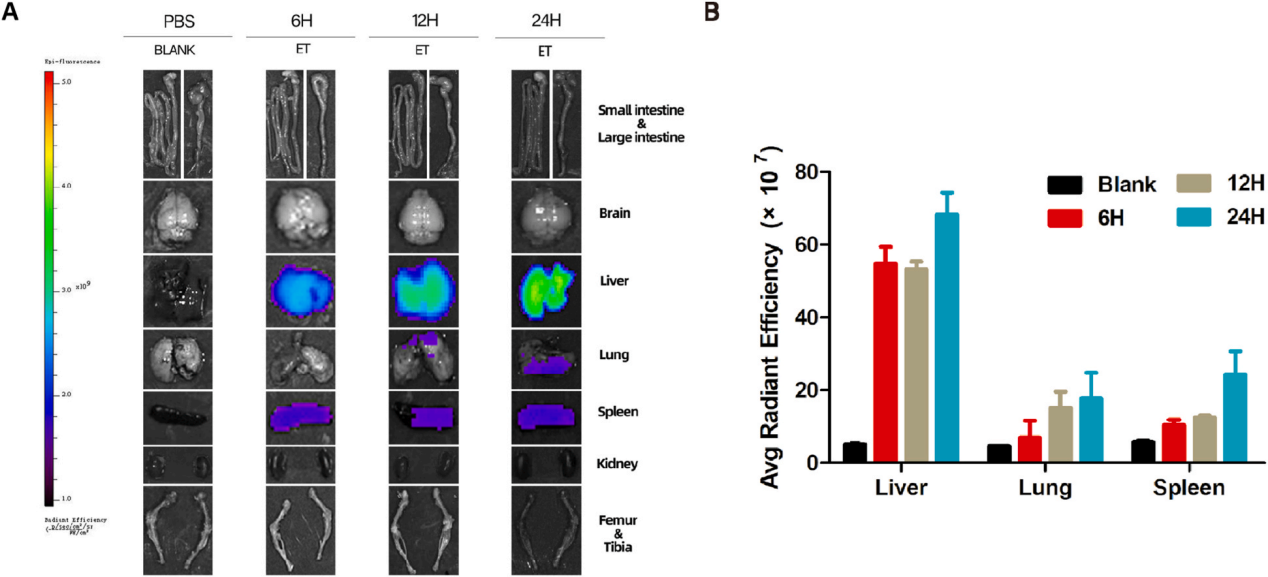
图4.小鼠RPM-ELNs的生物分布图像
本研究首次揭示了何首乌来源ELNs的抗肝癌活性及其分子机制,融合了传统中药与现代纳米技术,为肝癌治疗提供了新型天然纳米药物候选。其创新性在于从“天然产物分离-功能验证-机制解析-靶向性探索”的全链条研究模式,兼具基础科学与转化医学价值。未来研究可进一步优化ELNs的工程化修饰,提升其靶向性与疗效,推动临床前开发。
如果您正在探索:外泌体的提取和鉴定,癌症机制研究中的外泌体动态调控;植物来源外泌体的功能验证;外泌体生物标志物的筛选,请及时联系我们,获取免费技术咨询或定制方案设计!让我们以“纳米级智慧”,助您抢占科研与产业化的制高点!
参考文献
Mingqing Yanga ∙ Lining Xub ∙ Weiyu Wang. Molecular anti-tumorigenic mechanism of Radix Polygoni Multiflori-derived exosome-like nanoparticles. Heliyon, Volume 11, Issue 4, e41918.
最新动态
-
04.14
Int J Mol Sci | 植物性外泌体样纳米囊泡治疗早期骨关节炎的分离、表征和体外细胞研究
-
04.14
RNA pull down技术实验的应用场景
-
04.03
RIP技术如何破解RNA蛋白密码?
-
04.03
Food & Function:食用菌纳米囊泡突破-泌阳花菇提取物展现惊人辐射防护力
-
03.27
J. Adv. Res.|植物源性细胞外囊泡治疗IBD:多机制作用与药物载体潜力
-
03.27
植物外泌体:解锁中药未来的 “纳米密码”
-
03.20
细胞内的"GPS"追踪术:揭秘蛋白亚细胞定位的奥秘
-
03.20
BiFC技术,让蛋白互作“看得见”!
-
03.20
双荧光酶数据分析指南!!!
-
03.20
【合作文献分享】双剑合璧!外泌体研究新成果揭示癌症治疗新方向










